En fonction de l'angle de vue: nous pourrions n'observer rien de plus qu'un artefact de mesure d'anticorps.
Si nous supposons que tous les patients ne forment pas d'anticorps au même taux d'incidence mais tous les patients avec la même probabilité et un et même patient à vitesse constante, alors un effet d'immunogénicité assez simple peut être observé:
en administration constante, les anticorps sont simplement utilisés à une vitesse constante, étant actifs et liés, mais non libres et mesurables. Dans le traitement épisodique, le taux de production d'anticorps conduit alors à plus d'anticorps libres (non utilisés) à mesurer - et immédiatement disponibles pour une action contre le produit biologique, une fois qu'il est réintroduit dans le système.
Ainsi un une simple reformulation de la citation introductive de la question pourrait se lire
L'interruption du traitement d'entretien programmé anti-TNF ou du traitement épisodique a toujours été associée à des taux plus élevés de détection de formation d'anticorps .
Un article récent résume la situation comme suit:
Les options de traitement incluent les thérapies biologiques; cependant, une partie des patients perdent la réponse aux produits biologiques, en partie à cause de la formation d'anticorps anti-médicament (ADA). Les agents immunosuppresseurs concomitants réduisent le développement des ADAb.
Une recherche documentaire complète a été menée pour les articles publiés de janvier 2009 à août 2015 rapportant l'immunogénicité à l'adalimumab (ADM), au certolizumab pegol (CZP), au golimumab, à l'infliximab (IFX) , ustekinumab et vedolizumab dans les maladies inflammatoires de l'intestin (MICI).
Dans la plupart des études incluses qui évaluaient l'efficacité, la présence d'ADAb était associée à une réduction de l'efficacité. L’efficacité a été évaluée de diverses manières, y compris la réponse / rémission de l’indice d’activité de la maladie de Crohn (CDAI), la réponse Mayo, l’amélioration endoscopique et l’arrêt du traitement. Dans les études sur l'IFX, la proportion de patients obtenant et conservant une réponse était généralement plus faible chez les patients avec des ADAb détectés que chez ceux sans ADA détectés (tableau supplémentaire 7). Les ADAb à ADM étaient également associés à une efficacité réduite et une perte de réponse, ainsi qu'à un taux élevé d'échec du traitement secondaire; ces associations se sont révélées statistiquement significatives dans certaines études (tableau supplémentaire 8). Dans une étude26, l'arrêt du traitement par ADM a été très élevé (83,3%) chez les patients atteints d'ADAb (tableau supplémentaire 8).
Le moment du prélèvement (avant ou juste après la prochaine administration) influence grandement le taux de détection. La plupart des tests ne détectent pas les ADAb en présence de médicament; étant donné que la concentration du médicament est la plus faible juste avant la prochaine perfusion, c'est le moment optimal pour échantillonner. Cela pourrait être une explication de la formation d'ADAb signalée comme étant plus faible dans les ECR que dans les études observationnelles. . Cependant, il est également probable que les techniques d'analyse améliorées utilisées dans les études d'observation, ainsi que la sélection de patients présentant une perte de réponse, aient conduit à des niveaux de détection des ADAb plus élevés que dans les ECR.
Séverine Vermeire & Ann Gils & Paola Accossato & Sadiq Lula & Amy Marren: "Immunogénicité des produits biologiques dans les maladies inflammatoires de l'intestin", Therap Adv Gastroenterol. 2018; 11: 1756283X17750355. Publié en ligne le 21 janvier 2018. Doi: 10.1177 / 1756283X17750355, PMCID: PMC5784568, PMID: 29383030.
Le ci-dessus est juste une spéculation informée, espérons-le, basée sur le manque d'informations dans les articles étudiés sur la façon dont les anticorps ont été mesurés. Il s'agit de savoir si toutes ces valeurs possibles ont été prises: la concentration d'antigène, la concentration du complexe antigène-anticorps, les concentrations d'anticorps libres et / ou d'anticorps totaux.
La réaction antigène-anticorps est largement utilisée dans diagnostics de laboratoire, y compris l'immuno-hématologie. C'est une réaction chimique réversible:
antigène + anticorps ⇄ complexe antigène - anticorps
Les forces joignant le complexe antigène-anticorps ne sont pas des liaisons covalentes fortes mais des liaisons plus faibles, nommées à juste titre «faibles interactions ”.
Roberto Reverberi & Lorenzo Reverberi:" Facteurs affectant la réaction antigène-anticorps ", Blood Transfus. 2007 oct; 5 (4): 227–240. doi: 10.2450 / 2007.0047-07 PMCID: PMC2581910, PMID: 19204779
À la poursuite d'une oie sauvage : Encore plus spéculative pourrait être la pensée que dans ces processus un effet de renforcement continu par rapport à un renforcement intermittent se produit.
Un point à observer: l'infliximab est très différent des autres agents anti-TNF, car leurs attributs sont très différents:
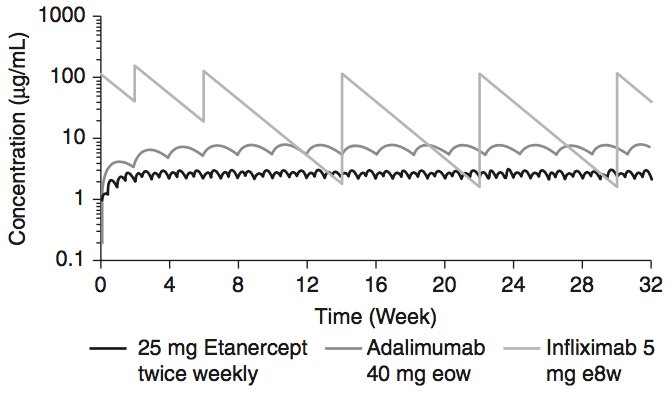
Une simulation pharmacocinétique des concentrations sériques d'infliximab, d'étanercept et adalimumab à l'état d'équilibre chez les patients atteints de PR traités avec chaque médicament aux doses et calendriers indiqués.
Les conséquences cliniques de l'immunogénicité des antagonistes du TNF comprennent une résistance acquise aux médicaments et des réactions au point de perfusion ou d'injection. Les anticorps anti-médicament peuvent former des complexes multivalents avec le médicament cible, entraînant une clairance et une inactivation rapides du médicament. Les stratégies pour y faire face comprennent l'augmentation de la dose ou l'ajout d'un traitement immunosuppresseur concomitant pour réduire la formation d'anticorps. Des études sur l'immunogénicité des médicaments à base de protéines ont suggéré que les anticorps chimériques sont généralement plus immunogènes que les anticorps humanisés ou humains. Cependant, les comparaisons du potentiel immunogène des agents anti-TNF sont difficiles, en grande partie à cause des différences de sensibilité des dosages conçus pour détecter les anticorps anti-médicaments, ainsi que de l'interférence dans les dosages du médicament lui-même.
Jennifer L. Jones: "Les agents anti-TNF sont-ils tous les mêmes?", dans: Peter M. Irving et al (Eds): "Clinical Dilemmas in Inflammatory Bowel Disease", Wiley-Blackwell: Chichester, Hobokem 2 2011.